一叶知秋 | 探秘 AGS 基因编辑细胞:解锁胃癌研究新密码
2025-05-20
1.细胞背景
胃癌是中国常见的恶性肿瘤之一,根据国家癌症中心发布的全国癌症统计数据,胃癌发病率和死亡率分别位于所有恶性肿瘤的第4位和第3位。早期胃癌多无症状或仅有轻微症状,当临床症状明显时,病变已发展到晚期,晚期胃癌仍缺乏有效的治疗手段。胃癌细胞系为研究胃癌的发展机制和防治手段提供了理想的体外模型,常见的人胃癌细胞系有SNU1, SNU16, AGS, KAT03, NCI-N87等。
AGS(人胃腺癌细胞)是从一名54岁的白人女性胃腺癌患者的胃组织中分离获得。1979 年由美国德克萨斯大学 MD 安德森癌症中心的 J. Fogh 等人通过原代培养建立,并于 1982 年正式命名为 “AGS”(取自患者姓名首字母缩写)。通过CRISPR基因编辑技术对AGS细胞进行靶向编辑,可精准解析特定基因在胃癌细胞发展中的功能,为疾病机制研究和药物开发提供关键工具。
2.细胞描述
物种:人
组织:胃
细胞形态:贴壁细胞,上皮细胞样
细胞倍增时间:~16-24 hours
培养条件
完全培养基成分:Ham's F-12K+10% FBS+1% P/S
培养环境:37℃、5%CO2
传代比例:1:3~1:4
传代频次:2~3 天传代一次
细胞形态图片
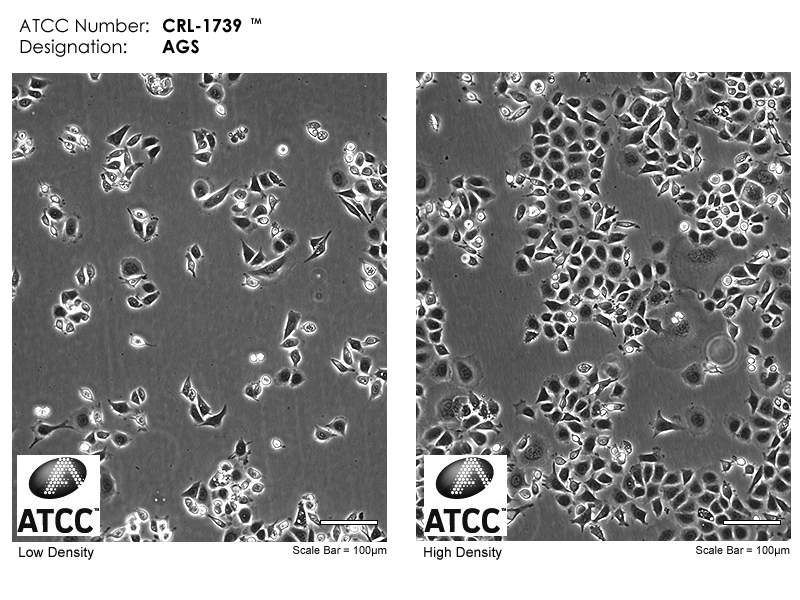
图1 AGS细胞参考ATCC正常形态图
细胞特点:
AGS细胞属于永生化细胞系,具有典型的上皮样形态,贴壁生长时呈多边形或铺路石样排列。细胞染色体数目为亚二倍体(约 44-52 条),存在多种染色体异常,如 17 号染色体三体、TP53 基因突变等。细胞贴壁紧密,生长速度快,汇合度达到70%-80%左右可传代(类似于下图36h密度)。
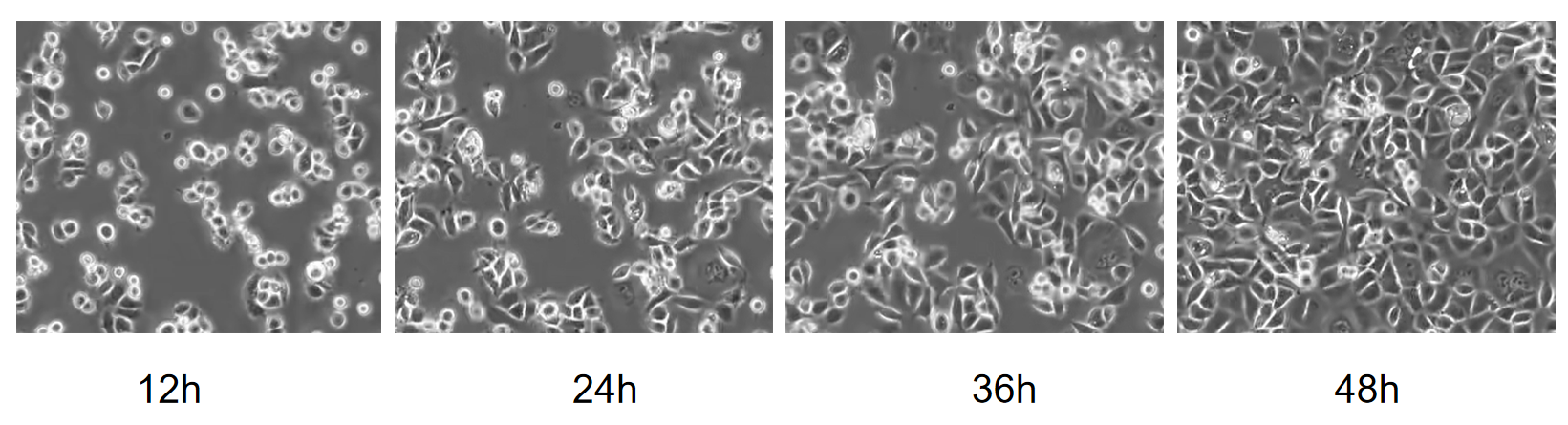
图2 AGS细胞生长图
3.粒曼AGS基因编辑细胞
针对某个或某一类基因构建敲除细胞系,可用于探索胃癌发病机制与潜在治疗靶点、评估新型靶向药物疗效、探索耐药机制、增强免疫治疗活性等。
例如,利用 CRISPR - Cas9 技术对 AGS 细胞中的 PIK3CA 基因进行编辑。敲除 PIK3CA 基因后,AGS 细胞的增殖、迁移和侵袭能力显著降低。这一发现不仅揭示了 PIK3CA 基因在胃癌进展中的重要作用,还提示 PI3K - AKT 信号通路可能成为胃癌治疗的潜在靶点。后续可研发针对该通路的抑制剂用于胃癌治疗。
另外,构建荧光蛋白过表达稳转AGS细胞系,可用于实时监测抗癌药物的活性或异体移植后肿瘤的发展进程。
粒曼生物积累了热门靶点的AGS敲除细胞及荧光蛋白过表达细胞,助力胃癌研究。
|
序号 |
类型 |
细胞名称 |
基因名称 |
实验方法 |
多克隆阳性率 |
单克隆阳性率 |
|
1 |
KO |
AGS |
PPFIA4 |
RNP |
90% |
100% |
|
2 |
KO |
AGS |
ADAM32 |
RNP |
95% |
100% |
|
3 |
KO |
AGS |
GPRC5C |
RNP |
95% |
100% |
|
4 |
KO |
AGS |
PPP1R18 |
RNP |
95% |
100% |
|
5 |
KO |
AGS |
SIVA1 |
RNP |
98% |
100% |
|
6 |
OE |
AGS_KO_SIVA1 |
GFP |
RNP |
95% |
100% |
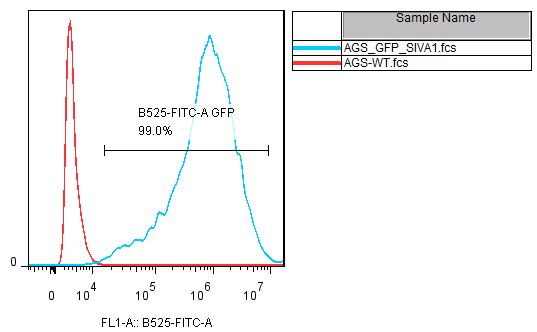
AGS_GFP_SIVA1 细胞的 GFP荧光表达流式分析结果示例:
2025 /
05-20
所属分类:
公司新闻
相关资讯—
2025-05-20
2025-05-20
2025-05-20

